ЧРЕСКОЖНЫЕ МИНИИНВАЗИВНЫЕ ВМЕШАТЕЛЬСТВА ПРИ ГНОЙНО-НЕКРОТИЧЕСКИХ ОСЛОЖНЕНИЯХ ОСТРОГО ДЕСТРУКТИВНОГО ПАНКРЕАТИТА (ДИС.К.М.Н.)
На правах рукописи
Мороз Ольга Владимировна
ЧРЕСКОЖНЫЕ МИНИИНВАЗИВНЫЕ ВМЕШАТЕЛЬСТВА
ПРИ ГНОЙНО-НЕКРОТИЧЕСКИХ ОСЛОЖНЕНИЯХ
ОСТРОГО ДЕСТРУКТИВНОГО ПАНКРЕАТИТА
14.01.17 – хирургия
14.01.13 – лучевая диагностика, лучевая
терапия
Автореферат
диссертации
на соискание ученой степени
кандидата
медицинских наук
Москва
– 2013
Работа выполнена в Государственном бюджетном
образовательном учреждении высшего профессионального образования «Московский
государственный медико-стоматологический университет имени А.И. Евдокимова»
Министерства здравоохранения Российской Федерации (ГБОУ ВПО МГМСУ им. А.И.
Евдокимова Минздрава России) на кафедре общей хирургии (заведующий кафедрой
д.м.н., профессор И.Ю. Яковенко). Ректор д.м.н., профессор, заслуженный врач РФ
О.О. Янушевич
Научные руководители:
доктор
медицинских наук, профессор, академик РАМН директор ФГБУ «Институт хирургии им.
А.В. Вишневского» Министерства здравоохранения России Кубышкин Валерий Алексеевич
доктор
медицинских наук, профессор кафедры факультетской хирургии №2 ГБОУ ВПО МГМСУ
им. А.И. Евдокимова Минздрава России Кулезнева
Юлия Валерьевна
Официальные оппоненты:
ЛУЦЕВИЧ Олег
Эммануилович, доктор медицинских наук, профессор, заведующий кафедрой факультетской
хирургии №1 ГБОУ ВПО МГМСУ им. А.И. Евдокимова Минздрава России
ЛЕМЕШКО Зинаида Ароновна,
доктор
медицинских наук, профессор кафедры пропедевтики внутренних болезней, главный
научный сотрудник лаборатории «Хрономедицина и новые технологии в клинике
внутренних болезней» НИЦ ГБОУ ВПО «Первый Московский государственный
медицинский университет им. И.М. Сеченова» Минздрава России
Ведущее учреждение: ГБУ «Научно-исследовательский институт скорой помощи имени Н.В. Склифосовского Департамента здравоохранения города Москвы».
Защита состоится «__»
2013г в 14.00 на заседании диссертационного совета Д208.041.02 при ГБОУ
ВПО «Московский государственный медико-стоматологический университет им. А.И.
Евдокимова» Минздрава России, по адресу
С диссертацией можно ознакомиться в библиотеке Университета по адресу:
Автореферат разослан «__»
Ученый секретарь
Диссертационного совета
д.м.н., профессор Ярема Владимир Иванович
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы
В настоящее
время острый панкреатит (ОП) занимает 3-е место (12,5%) в структуре острых
хирургических заболеваний органов брюшной полости с тенденцией дальнейшего
роста заболеваемости и увеличением количества его деструктивных форм,
сопровождающихся большим числом осложнений и высокими цифрами летальности. Смертность при
деструктивных формах ОП на протяжении последних 40 лет не изменилась, она
примерно одинакова, как в нашей
стране, так и за рубежом и составляет по данным различных авторов 3,9% - 21% (Buchler M.W. с соавт., 2000; Савельев B.C. с соавт.,
2003; Ермолов А.С. с соавт., 2008).
Очевидные на сегодняшний день успехи интенсивной терапии и улучшение
результатов лечения больных панкреонекрозом в фазу панкреатического шока и
гемодинамических нарушений привели к тому, что статистически чаще (по сравнению
с предыдущим десятилетием) хирурги стали встречаться с разнообразными по
характеру и объему гнойно-некротическими осложнениями деструктивного
панкреатита. (Затевахин И.И. с соавт., 2002). Разнообразие течения
деструктивного панкреатита связано с особенностями топографической анатомии
поджелудочной железы и патогенезом заболевания. Это обусловливает трудности не
только ранней верификации патологических процессов, но и выбора метода
хирургического лечения. Этим же объясняется неоднородная и противоречивая
статистика результатов хирургического лечения данного контингента больных.
Дискутабельными остаются вопросы дифференцировки асептического и
септического процессов при ОП и, соответственно, хирургической тактики при этих
двух принципиально разных состояниях. Различная степень распространенности и
глубины некротического поражения самой поджелудочной железы, различных областей
обширной забрюшинной клетчатки, а также трансформация асептического некроза в
инфицированный определяют потенциальное многообразие вариантов хирургической
тактики, описанной в современной литературе. Так,
P. Gotzinger (2002) является сторонником активного
хирургического лечения любых форм панкреонекроза и рекомендует выполнение
радикальных операции. Некоторые исследователи (Иванов П.А., 2002; Шуркалин
Б.К., 2005; Werner J., 2003) считают, что пункционно-дренирующие вмешательства под
ультразвуковым наведением стали альтернативой традиционным хирургическим
способам лечения и должны их практически полностью заменить. Другие авторы (Johnson C.D., 2004; Lindkvist B., 2004 ; Banks P.A., 2006) предлагают различные сочетания традиционных лапаротомий с
миниинвазивными вмешательствами.
В целом существенных положительных сдвигов в
неотложной панкреатологии за последние десятилетия не произошло. Существуют разные концепции, касающиеся тактики ведения больных с
деструктивным панкреатитом, – от различных вариантов консервативного лечения в
ранние сроки заболевания до разнообразных хирургических вмешательств на
поджелудочной железе и забрюшинном пространстве при гнойно-септических
осложнениях. Следовательно, вопрос о том, какому методу оперативного лечения
деструктивного панкреатита и его септических осложнений следует сегодня
отдавать предпочтение, остается нерешенным. Также до конца не определена роль и
место чрескожных миниинвазивных технологий под контролем ультразвукового
исследования и рентгенотелевидения в лечении гнойно-некротических осложнений.
Таким
образом, вышеизложенное
обусловливает актуальность проведения диссертационного исследования.
Цель исследования:
определение
критериев эффективности, продолжительности и
целесообразности применения только миниинвазивного лечения
деструктивного панкреатита в стадии гнойно-некротических осложнений.
Задачи
1.
Определить роль
клинико-лабораторных и лучевых методов диагностики некротического панкреатита и
его осложнений на разных стадиях течения заболевания.
2.
Уточнить ультразвуковую семиотику
гнойно-некротических осложнений острого
панкреатита.
3.
Обосновать показания к
выполнению чрескожных миниинвазивных вмешательств под контролем УЗИ и рентгенотелевидения
во второй фазе течения деструктивного панкреатита.
4.
Оценить результаты
чрескожных дренирующих операций при различных осложнениях деструктивного
панкреатита в фазе гнойно-некротических осложнений.
5.
Провести сравнительный
анализ традиционных и чрескожных миниинвазивных вмешательств при деструктивном
панкреатите в стадии гнойно-некротических осложнений.
Научная новизна
Выявлены
клинико-лабораторные и инструментальные критерии развития гнойно-некротических
осложнений острого деструктивного панкреатита.
Установлены
роль и границы возможностей миниинвазивных вмешательств в хирургии
гнойно-некротических осложнений острого деструктивного панкреатита.
На
основании клинико-лабораторных показателей течения заболевания и результатах
лечения доказаны преимущества миниинвазивных вмешательств перед традиционными оперативными
вмешательствами при гнойно-некротических осложнениях острого деструктивного
панкреатита в достоверно сопоставимых группах.
Практическая
значимость
Произведена
оценка информативности клинико-лабораторных показателей и данных
ультразвукового исследования при выявлении гнойно-некротических осложнений
деструктивного панкреатита.
Проанализированы
особенности выполнения миниинвазивных вмешательств в зависимости от характера выявленных
жидкостных скоплений поджелудочной железы и забрюшинной клетчатки.
Произведена
оценка особенностей и длительности послеоперационного периода, а также уровня
летальности у больных с гнойно-некротическими осложнениями деструктивного
панкреатита, прооперированных миниинвазивно и традиционными способами.
Основные положения диссертации, выносимые
на защиту:
1. Ультразвуковое
исследование в совокупности с клинико-лабораторными данными является
информативным методом диагностики выявления гнойно-некротических осложнений
деструктивного панкреатита.
2. Миниинвазивные
вмешательства всегда можно использовать как первый этап хирургического лечения
у больных с гнойно-некротическими осложнениями деструктивного панкреатита.
3. При
длительно сохраняющемся интоксикационном синдроме после пункционно-дренажного
лечения необходимо решение вопроса о некрсеквестрэктомии традиционным способом.
Апробация работы
Основные
положения диссертации представлены на:
1.
VI Всероссийском
национальном конгрессе лучевых диагностов и терапевтов. Радиология – 2012 (Москва);
2.
IX научно-практической
конференции радиологов Узбекистана «Современные методы медицинской визуализации
и интервенционной радиологии»,
3.
II съезде российского
общества хирургов гастроэнтерологов,
4.
10th Congress
Europian-African Hepato Pancreato Biliary Assosiation,
5.
совместном заседании кафедр
общей хирургии, факультетской хирургии №2, лучевой диагностики лечебного
факультета, кафедры хирургии факультета последипломного образования ФПДО ГБОУ
ВПО «Московский государственный медико-стоматологический университет им. А.И.
Евдокимова» Минздрава России и кафедры хирургии факультета фундаментальной
медицины Московского государственного университета им. М.В. Ломоносова (
Степень личного участия в работе
Личное
участие соискателя в работе составляет более 80%. Основано на самостоятельном
ведении пациентов с острым деструктивным панкреатитом, участии в операциях,
выполняемых миниинвазивно и традиционным способом в качестве оператора и
ассистента; личном анализе всех историй болезни, журнала учета исследований и
прочей медицинской документации; статистической обработке полученных данных;
написании научных статей, выступлении на научно-практических конференциях с
докладом результатов исследований; написании и оформлении диссертационной
работы.
Публикации
По теме диссертации опубликовано
11 печатных работ (из них 3 статьи в
журналах, рекомендованных ВАК).
Внедрение результатов исследования в практику
Результаты
исследования внедрены в практическую деятельность ГКБ №68, ГКБ №29, КБ №119
ФМБА, Дорожной больницы им. С.В. Семашко на станции «Люблино». Также результаты
исследования используют в качестве лекционного материала на кафедрах общей
хирургии лечебного факультета и факультетской хирургии №2 МГМСУ им. А.И. Евдокимова,
хирургии факультета фундаментальной медицины МГУ им. М.В. Ломоносова.
Объем и структура работы
Работа
состоит из введения, четырех глав, заключения,
выводов, практических рекомендаций и библиографического указателя; изложена на
150 страницах, иллюстрирована 22 рисунками, 7
диаграммами и 14 таблицами. Библиографический указатель представлен 239 источниками, из них 128 - иностранных авторов.
СОДЕРЖАНИЕ
РАБОТЫ
Исследование основано на результатах
хирургического лечения 115 пациентов деструктивным панкреатитом с развившимися
гнойно-некротическими осложнениями заболевания, находившихся на лечении в ГКБ
№68 г. Москвы. Пациенты были разделены на две группы в зависимости от способа
оперативного лечения. Первую
составили 33 (28,7%) пациента, у которых традиционное вмешательство выполняли
как основной метод хирургического лечения. Во вторую группу вошли 82 (71,3%) пациента, у которых
хирургическое лечение начинали с миниинвазивных чрескожных вмешательств.
В обеих группах пациенты были сопоставимы
по возрасту, полу, этиологии заболевания и сопутствующей патологии.
Сравнительную оценку проводили при помощи корреляционного анализа путем
сравнения сумм рангов.
Средний возраст пациентов составил
46,7±1,5 года. Соотношение мужчин и женщин в группах было 1:0,45 и 1:0,48
соответственно. Распределение больных по этиологическому фактору представлено в
таблице 1.
Таблица 1
Распределение больных по
этиологическому фактору
|
Причина развития панкреатита |
1-ая группа |
2-ая группа |
Статистическая значимость |
|
Алкогольно-алиментарный фактор |
20 (60,6%) |
49 (59,7%) |
p=0,85 |
|
Желочнокаменная болезнь |
4 (12,1%) |
11 (13,4%) |
p=0,76 |
|
Травма |
2 (6,0%) |
5 (6,1%) |
p=0,98 |
|
По неустановленной причине |
6 (18,1%) |
17 (20,7%) |
p=0,68 |
|
Всего больных |
33 (100%) |
82 (100%) |
|
Данные
приведенные в таблице свидетельствуют о сопоставимости групп по этиологическому
фактору развития деструктивного панкреатита (p > 0,05).
Наиболее частой причиной деструктивного панкреатита был алкогольно-алиментарный
фактор: в 1-й группе 56,4%, во 2-й группе - 60,3%.
По сопутствующим заболеваниям, как приведено в таблице
2, группы больных сопоставимы.
Для сравнительной оценки эффективности
лечения больных в 1-й и 2-й группах использовали классификацию острого
панкреатита, основанную на данных лучевой диагностики, принятую в
Постнекротические панкреатические и
парапакреатические жидкостные скопления в зависимости от содержимого были
разделены на:
·
инфицированный некроз без выраженного жидкостного компонента;
·
с преимущественно экссудативным компонентом (флюктуирующее);
·
с преимущественно некротическим компонентом (секвестрами).
Таблица 2
Распределение больных по
сопутствующим заболеваниям
|
Сопутствующие заболевания |
1-ая группа |
2-ая группа |
Статистическая значимость |
|
ЖКБ: хронический калькулезный холецистит |
4 (12,1%) |
10 (12,2%) |
p=0,89 |
|
Хронический гастродуоденит |
3 (9,0%) |
7 (8.5%) |
p=0,75 |
|
Хронический пиелонефрит |
1 (3,0%) |
3 (3,6%) |
p=0,67 |
|
ИБС: атеросклеротический коронарокардиосклероз |
3 (9,0%) |
9 (10,9%) |
p=0,85 |
|
Сахарный диабет II
типа |
3 (9,0%) |
7 (8,5%) |
p=0,37 |
|
Хроническая алкогольная интоксикация |
6 (18,1%) |
15 (18,2%) |
p=0,84 |
|
Сопутствующие заболевания |
4 (12,1%) |
10 (12,2%) |
p=0,28 |
|
Без сопутствующих заболеваний |
9 (27,2%) |
21 (25,6%) |
p=0,87 |
|
Всего |
33 (100%) |
82 (100%) |
|
В каждой из групп
пациенты были разделены на подгруппы по степени тяжести острого панкреатита.
При разделении больных на данные категории использовали классификацию
В.И. Филина – А.Д. Толстого, согласно которой к больным со средней степенью
тяжести в фазе гнойно-некротических осложнений относят пациентов с единичными
абсцессами различной локализации, а с тяжелым состоянием – больных со сливной
секвестральной флегмоной парапанкреатической клетчатки в пределах сальниковой
сумки и распространяющейся за пределы сальниковой сумки: по левому и/или
правому флангам и/или корню брыжейки.
Для определения гнойно-некротических
осложнений в фазе секвестрации оценивали следующие проявления:
·
клинические (болевой
синдром, рвота, не приносящая облегчение, желтуха, лихорадка, пульс, систолическое
артериальное давление, частота дыхательных движений);
·
лабораторные данные (общий и биохимический
анализ крови);
·
инструментальные
методы исследования (ультразвуковое исследование (УЗИ), электрокардиография,
эзофагогастродуоденоскопия, рентгенография органов грудной клетки).
Для определения значимости клинико-лабораторных и
инструментальных признаков использовали корреляционный анализ с вычислением коэффициента линейной корреляции Пирсона (R) и коэффициент ранговой корреляции Спирмена (Rs); проводили
анализ таблиц сопряжённости, линейный и ранговый корреляционный анализ с
критерием уровня значимости, равном 5%. Анализ данных производили с помощью
пакета прикладных программ Statistica for Windows 6,0 на ПВЭМ. В зависимости от
вида шкалы измерения применяли следующие методы определения связи признаков:
·
таблицы сопряженности для изучения связи
признаков вида «да или нет»;
·
коэффициенты корреляции Спирмена и Кендела
для признаков, измеренных в порядковой шкале - данных типа «лучше - хуже» и
тестовых баллов;
·
коэффициент корреляции Пирсона для данных,
измеренных в количественных шкалах.
Проверку нормальности
распределения количественных признаков производили с использованием критерия
Колмогорова-Смирнова.
При малом числе наблюдений (до 30)
использовали непараметрические методы оценки значимости различий: непараметрический
критерий Пирсона хи-квадрат, U критерий
Манна-Уитни, двухвыборочный критерий Колмогорова-Смирнова, Т-критерий
Вилкоксона, коэффициент ранговой корреляции Спирмена.
Результаты
исследования и их обсуждение
С целью определения информативности
клинико-лабораторных и инструментальных данных использовали ряд диагностических
признаков. Исследование проводили у всех пациентов обеих групп
вне зависимости от степени тяжести, поскольку основной задачей было определение
признаков, характерных для развития гнойно-некротических осложнений, а не
выявление различий между группами. На
основании проведенного анализа было выявлено, что сильную статистическую связь
имеет следующие параметры:
1. клинические признаки:
·
лихорадка (выше 38,6 градусов);
·
частота сердечных сокращений (более 100 в 1 минуту);
·
частота дыхательных движений (более 20 в 1 минуту);
2. лабораторные показатели:
·
лейкоцитоз (более 14 х109/л);
·
лимфопения (менее 10 х109/л);
·
уровень общего белка крови (менее 60 г/л);
·
уровень глюкозы крови (более 8 ммоль/л);
3. инструментальные данные:
·
реактивный плеврит;
·
нижнедолевая пневмония.
При статистической обработке данных
было установлено, что появление этих показателей является признаками
инфицирования уже существующих зон деструкции поджелудочной
железы и/или забрюшинного пространства.
УЗИ выполняли всем
больным при поступлении и в дальнейшем по показаниям в зависимости от
клинико-лабораторной картины. При развитии гнойно-некротических осложнений
среднее число исследований составило 10±2,3, частота выполнения исследований
была не менее 1-2 раз в неделю, при необходимости – ежедневно.
Анализ
результатов исследования позволил разработать порядок проведения
ультразвукового исследования, которое должно включать в себя:
1.
осмотр паренхимы железы;
2.
исследование клетчаточных пространств;
3.
определение свободной жидкости в брюшной полости;
4.
оценку состояния органов брюшной полости и почек;
5.
осмотр плевральных полостей.
Результаты УЗИ в
последующем сравнивали с результатами фистулографии в ходе проведения
диагностической пункции и/или дренирования, что позволило выявить ряд
характерных особенностей.
Оценка
состояния поджелудочной железы показала, что чаще она была увеличена в размерах
- 95 (81,1%), имела нечеткие, неровные контуры - 98 (86,9%) и неоднородную
структуру - 93%. Однако, в 20 (17,9%) случаях железа имела нормальные размеры и
эхоструктуру.
При выявлении зон деструкции в клетчаточных пространствах
определяли их форму, размеры, контуры и структуру. Структура зоны некроза могла
меняться в зависимости от стадии патологического процесса: от инфильтрата до
полного гнойного расплавления жировой клетчатки в этой области. В ходе анализа
полученных данных для каждого вида деструкции были установлены характерные
ультразвуковые и рентгенологические признаки.
Инфицированный некроз
без выраженного жидкостного компонента.
При УЗИ в забрюшинной
клетчатке определяли гиперэхогенную зону с нечеткими, неровными контурами,
различных размеров и конфигурации с линейными прослойками жидкости (рис. 1а).
Особенности
рентгенологической картины при фистулографии: пропитывание забрюшинной
клетчатки по типу «пчелиных сот» без четких контуров и границ. Полного
отграничения зоны деструкции еще не произошло, поэтому на данном этапе
патологического процесса она имели полигональные формы со множеством отрогов (рис.
1б).
а б
Рис. 1. Инфицированный некроз параколической клетчатки: а
- УЗ-картина слева; б - рентгенологическая картина справа.
Жидкостные скопления с преимущественно
жидкостным содержимым.
Данный вид жидкостных
скоплений при УЗИ имел овальную или округлую форму, четкие, довольно ровные
контуры. В структуре жидкостного скопления визуализировали мелкие гиперэхогенные
включения, флюктуирующие при компрессии датчиком. Некротический компонент либо
полностью отсутствовал, либо был представлен единичными мелкими гиперэхогенными
включениями размером до 5-
При
фистулографии определяли полость с четкими, довольно ровными контурами,
овальной или округлой формы и умеренно неоднородным контрастированием (рис. 2б).
а б
Рис. 2. Жидкостное скопление с
преимущественно жидкостным содержимым: а - УЗ-картина; б - рентгенологическая
картина
Жидкостные скопления с преимущественно
некротическим компонентом.
Данный вид жидкостных
скоплений при УЗИ имел нечеткие неровные контуры, овальную или округлую форму.
В просвете скопления визуализировали неоднородное содержимое за счет наличия гиперэхогенных
включений, не окрашиваемых при дуплексном сканировании (рис. 3а). Эти включения
могли занимать объем более, чем на 50% относительно экссудативного компонента.
При фистулографии определяли
полость с нечеткими, неровными контурами с множеством дефектов контрастирования
(секвестрами), фиксированными по краю образования, либо свободно лежащими и
смещаемыми в просвете (рис. 3б).
а б
Рис. 3. Жидкостное скопление с
преимущественно некротическим компонентом: а - УЗ-картина; б - рентгенологическая
картина
В обеих группах
преобладали пациенты, имевшие жидкостные скопления с преимущественно некротическим
компонентом (секвестрами), расположенные
в парапанкреатической и параколической клетчатке.
Жидкостные
скопления встречались в различных сочетаниях, как показано в таблице 3.
Таблица 3
Сочетание областей
поражения при различных видах некроза забрюшинной клетчатки
|
Область
поражения |
Состояние |
Всего |
|
|
Ср.
тяжести |
Тяжелое |
||
|
Парапанкреатическая
клетчатка |
1 (3%) |
0 |
1 |
|
Параколическая
клетчатка |
3 (9%) |
2 (6%) |
5 |
|
Парапанкреатическая клетчатка + Параколическая клетчатка |
2 (6%) |
5 (15%) |
7 |
|
Свободная жидкость в брюшной полости |
2 (6%) |
4 (12%) |
6 |
|
Парапанкреатическая клетчатка + Свободная жидкость в брюшной полости |
1 (3%) |
7 (21%) |
8 |
|
Параколическая клетчатка + Свободная жидкость в брюшной полости |
2 (6%) |
3 (9%) |
5 |
|
Парапанкреатическая клетчатка + Параколическая клетчатка + Свободная жидкость в брюшной полости |
0 |
1 (3%) |
1 |
|
Всего |
11 |
22 |
33 |
Общий
анализ результатов инструментальных методов показал, что полноценное,
динамическое УЗ-исследование органов брюшной полости позволяет выявить как
основные признаки заболевания, так и определить осложнения со стороны других
органов и систем. УЗИ необходимо производить в полном объеме по всем пунктам
протокола, как при первичном, так и при динамическом осмотре, поскольку
развитие дополнительных осложнений возможно на всех этапах течения
деструктивного процесса. Выраженность УЗ-признаков при гнойно-некротических
осложнениях показана в таблице 4.
Таблица 4
Ультразвуковые признаки
острого деструктивного панкреатита в фазу гнойно-некротических осложнений
|
Ультразвуковые признаки |
Выраженность |
|
Увеличение размеров, размытость, неоднородность
структуры ПЖ |
94 (82,2%) |
|
Инфицированный некроз и ЖС в парапанкреатической
клетчатке |
88 (65,2%) |
|
Инфицированный некроз и ЖС в параколических
клетчаточных пространствах |
37
32,%) |
|
Свободная жидкость в брюшной полости |
33 (28,8%) |
|
Расширение желчных протоков |
5 (4,3%) |
|
Осложнения со стороны других органов брюшной полости |
2 (1,8%) |
|
Выпот в плевральных полостях |
9 (7,8 %) |
Таким образом, при
ретроспективном анализе историй болезни были установлены следующие достоверные
признаки гнойно-некротических осложнений деструктивного панкреатита,
развивающиеся в среднем на 16±1,5 сутки от начала заболевания:
1. Клинические:
·
лихорадка выше 38,6 градусов;
·
частота сердечных сокращений (более 100
в 1 мин.);
·
частота дыхательных движений (более 100
в 1 мин.);
2. Лабораторные:
·
лейкоцитоз более 14 х 109/л;
·
лимфопения менее 1.2 х 109/л;
·
общий белок менее 60 г/л;
·
глюкоза крови более 8 ммоль/л;
3. Рентгенологические:
·
реактивный плеврит;
·
нижнедолевая пневмония;
4. Ультразвуковые:
·
увеличение размеров, размытость, неоднородность
структуры поджелудочной железы,
·
жидкостные скопления различной структуры в клетчаточных
пространствах,
·
свободная жидкость в брюшной полости.
Выявление этих
признаков является основанием для выполнения хирургического вмешательства
традиционным или миниинвазивным способом.
Открытые оперативные вмешательства
выполнены у 33 больных. При выборе открытого оперативного доступа
ориентировались на расположение зоны деструкции:
1.
при деструкции в парапанкреатической
клетчатке производили лапаротомию, ревизию, секвестрэктомию и санацию
сальниковой сумки, санацию и дренирование брюшной полости;
2.
при деструкции в параколической клетчатке
выполняли ее ревизию с соответствующей стороны, секвестрэктомию, санацию и
дренирование зон гнойного расплавления лапаротомным либо люмботомическим
доступом;
3.
при наличии осложнений со стороны других
органов брюшной полости после ревизии проводили симультанные операции на
желчном пузыре и внепеченочных желчных путях, селезенке.
Характер и число
выполненных операций представлено в таблице 5.
Программированные этапные санации брюшной
полости, парапанкреатической и параколической клетчатки производили с
интервалом 24 - 48 - 72 часа, либо по требованию.
У 33 больных, прооперированных традиционным
способом, было произведено 120 плановых санаций. В среднем на одного больного
приходилось 3-4 санации.
Таблица 5
Традиционные оперативные
вмешательства, выполняемые больным первой группы
|
Характер операций |
Число больных
в группе |
|
|
n |
% |
|
|
Лапаротомия,
санация и дренирование брюшной полости, некрсеквестрэктомия,
оментобурсостомия |
10 |
28.3 |
|
Лапаротомия,
холецистостомия/холецистэктомия, санация и дренирование брюшной полости,
оментобурсостомия |
3 |
10.2 |
|
Лапаротомия,
некрсеквестрэктомия, вскрытие параколической клетчатки, некрсеквестрэктомия,
дренирование, оментобурсостомия |
2 |
7.7 |
|
Лапаротомия,
некрсеквестрэктомия, дренирование сальниковой сумки; люмботомия, дренирование
флегмоны забрюшинного пространства |
3 |
10.2 |
|
Люмботомия
слева, некрсеквестрэктомия, дренирование забрюшинной клетчатки
, |
5 |
15.4 |
|
Люмботомия
справа некрсеквестрэктомия, дренирование забрюшинной клетчатки
|
3 |
7.7 |
|
Люмботомия
справа и слева некрсеквестрэктомия, дренирование забрюшинной клетчатки |
7 |
20.5 |
|
Всего |
33 |
100.0 |
По данным анализа, осложнения в
послеоперационном периоде случились у 6 больных. Характер осложнений и их
распределение в зависимости от степени тяжести представлено в таблице 6.
Таблица 6
Виды осложнений в
послеоперационном периоде у больных первой группы
|
Тип осложнения |
Тяжесть состояния
больных |
Всего |
|
|
Ср.
тяжести |
Тяжелое |
||
|
Аррозионное кровотечение |
1 |
4 |
5 |
|
Толстокишечный свищ |
0 |
1 |
1 |
|
Панкреатический свищ |
0 |
0 |
0 |
|
Всего |
1 |
5 |
6 |
Продолжительность пребывания больных в
стационаре в группе со средней степенью тяжести составила 30,2±5,4, а в группе
с тяжелым состоянием - 51,1±9,2.
Среди прооперированных традиционным
способом было 13 (39,3%) летальных исходов.В группе со средней степенью тяжести
летальный исход был в 1 случае вследствие аррозионного кровотечения в
послеоперационном периоде.
В группе с тяжелым
состоянием летальность составила 36,3%
(12 случаев): вследствие аррозионного кровотечения в послеоперационном периоде
(2), от явлений нарастающей полиорганной недостаточности (10).
Таким образом, в группе
с традиционными хирургическими вмешательствами при гнойно-некротических
осложнениях деструктивного панкреатита преобладали больные с инфицированным
некрозом и жидкостными скоплениями с секвестрами, с тяжелым состоянием, что
сопровождалось высокими цифрами летальности.
Для лечения больных 2-й группы
использовали чрескожные миниинвазивные дренирующие вмешательства.
Доступ для дренирования зависел от локализации скопления:
1.
внебрюшинный – 40 (48,8%) больных;
2.
через брюшную полость – 29 (35,4%) пациентов;
3.
чреспеченочный – 7 (8,5%) (при локализации
зоны деструкции в проекции головки поджелудочной железы);
4.
через паренхиму селезенки – 2 (2,4%) (вмешательство
ограничилось выполнением лечебно-диагностической пункции);
5.
чрезжелудочный – 4 (4,9%) (у 3-х больных вторым
этапом после получения продукции панкреатического сока наружный дренаж был
переведен во внутренний).
Выполнение вмешательств имело ряд
особенностей в зависимости от вида гнойно-некротических осложнений.
Особенностью дренирования инфицированного некроза без жидкостного
компонента являлось то, что во время диагностической пункции гной получали лишь при
активной аспирации в объеме 3–5 мл. Это было показанием для установки дренажей
большого диаметра типа «корзина» (18 – 28 Fr) с целью адекватного оттока гнойного экссудата и детрита, а также
возможности последующей некрсеквестрэктомии.
При инфицированном некрозе выполнено 14
миниинвазивных вмешательств. У 4 больных вследствие неэффективности
миниинвазивного лечения были выполнены открытые хирургические вмешательства —
лапаротомия, вскрытие, санация и дренирование очагов деструкции. В 2 случаях
лапаротомию выполняли по поводу аррозионного кровотечения. В 2 других — вследствие
неэффективности миниинвазивного лечения и нарастания признаков интоксикации.
Другими осложнениями в данной группе были:
толстокишечный свищ – в 3 случаях, панкреатический свищ – в 1. У всех больных
лечение толстокишечного и панкреатического свищей было консервативным.
Скопления с преимущественно жидкостным компонентом не имели крупных
фрагментов некротизированной ткани, поэтому диаметр дренажа мог быть не более
14 Fr. В этих случаях, как правило, удавалось добиться
быстрой санации полости.
При жидкостных скоплениях с преобладанием
флюктуирующего содержимого выполнено 17 миниинвазивных вмешательств;
пункционно-дренажное лечение было дополнено открытой операцией вследствие
фибринозно-гнойного перитонита в 2 случаях. Лечение самих жидкостных скоплений
не потребовало дополнительных способов лечения.
Среди осложнений отмечены: аррозионное
кровотечение –1; толстокишечный свищ –3; панкреатический свищ –1. Все
осложнения были ликвидированы консервативно.
Жидкостные скопления с преимущественным некротическим компонентом были дренированы
дренажами большого диаметра типа «корзинка» (18 – 28 Fr). Число дренажей было не ограничено и соответствовало числу недренируемых
полостей.
При этом типе жидкостных скоплений
выполнено 58 миниинвазивных вмешательств, пункционно-дренажное лечение было
дополнено открытым оперативным лечением в 10 случаях: вследствие аррозионного
кровотечения - в 2, вследствие нарастаний явлений полиорганной недостаточности -
в 8. Среди открытых оперативных вмешательств 6 пациентам была выполнена
срединная лапаротомия, люмботомия использована в качестве оперативного доступа у
4 больных. Среди других осложнений в послеоперационном периоде выявлены: толстокишечный
свищ – в 5 случаях; панкреатический свищ – в 1. Больные были пролеченные
консервативным способом.
Чресфистульная
секвестрэктомия
Как показало исследование, залогом успеха миниинвазивных
вмешательств при гнойно-некротических осложнениях является выполнение
ежедневных санации всех дренажей и поэтапной чресфистульной секвестрэктомии,
которая производится под рентгенотелевизионным контролем.
Методика выполнения чресфистульной секвестрэктомии. При
интенсивном промывании полости деструкции край секвестра «застревал» в корзинке
дренажа. Дренаж вращали в любую сторону, дополнительно накручивая секвестр
на корзинку. После этого дренаж на
проводнике извлекали вместе с фрагментом некротизированной ткани (рис. 4).
а б
Рис.4. Удаление фрагментов
некротизированной клетчатки с помощью дренажа типа «корзинка» 22 Fr (а и б –
различные варианты извлечённых секвестров)
Манипуляцию повторяли, пока не извлекали все
свободно лежащие на данный момент секвестры, а в последующем – ежедневно до
полной их эвакуации. Послеоперационные осложнения у больных 2-й группы
представлены в таблице 7.
Таблица 7
Послеоперационные
осложнения у больных 2-й группы
|
Тип осложнения |
Тяжесть состояния |
Всего |
|
|
Ср.
тяжести |
Тяжелое |
||
|
Аррозионное кровотечение |
4 |
1 |
5 |
|
Толстокишечный свищ |
3 |
8 |
11 |
|
Панкреатический свищ |
1 |
2 |
3 |
|
Всего |
8 |
11 |
19 |
Во 2-й группе преобладали пациенты со
средней степенью тяжести и единичными жидкостными скоплениями – 45 (54,8%). Общая
летальность составила 23% (19 больных).
В
группе со средней степенью тяжести было 4 летальных исхода вследствие аррозионного кровотечения в послеоперационном
периоде (2) и от явлений нарастающей полиорганной недостаточности (2).
В
группе с тяжелым состоянием летальных исходов было 15: вследствие аррозионного
кровотечения в послеоперационном периоде (1) и от явлений нарастающей
полиорганной недостаточности (14).
Койко-день
в группе со средней степенью тяжести составил 55,3±4,2, а в группе с тяжелым
состоянием больных - 70,9±6,7.
В
ходе исследования установлено, что 65 (56,5%) пациентов с гнойно-некротическими
осложнениями деструктивного панкреатита успешно пролечены при использовании
только миниинвазивных методик.
Анализ
результатов лечения данной группы больных позволил выявить следующие
закономерности.
1.
Наиболее благоприятно послеоперационный
период протекал у больных с единичными жидкостными скоплениями и с
флюктуирующим (гнойным) содержимым. У таких пациентов постоянное промывание
деструктивных очагов, наряду с проводимой консервативной
терапией, приводило к достаточно быстрому очищению и уменьшению полостей в
размерах.
2.
У пациентов с
инфицированным некрозом без жидкостного компонента и с секвестрами в жидкостных
скоплениях послеоперационный период протекал тяжелее как со стороны общего
состояния, так и со стороны местных изменений в забрюшинном пространстве.
Преобладание секвестров в очаге деструкции было причиной медленного очищения
полости от секвестров и, как следствие, сохранения интоксикации на протяжении
длительного времени. Зачастую это приводило к дальнейшему распространение
некроза по забрюшинной клетчатке и являлось причиной образования новых очагов
деструкции.
В
17 случаях миниинвазивное лечение оказалось неэффективным и потребовало
дополнительного хирургического вмешательства открытым доступом. В 11 случаях
операции выполнены в сроки более 20 дней от первого хирургического
вмешательства, это закончилось летальным исходом в 64,7% случаев.
Сравнение
результатов лечения обеих групп больных представлено в таблице 8.
Таблица 8
Результаты лечения
больных 1-й и 2-й групп
|
Показатели |
1-я группа |
2-я группа |
|
Осложнения |
6 (18,1%) |
19 (23,1%) |
|
Летальность |
13 (39%) |
19 (23,1%) |
|
Койко-день |
40,1 ± 5,3 |
60,5 ± 4,2 |
Из таблицы видно, что летальность во 2
группе была в 2 раза ниже, а продолжительность стационарного лечения
практически в 1,5 раза выше.
На основе полученных результатов был выведен следующий лечебный алгоритм ведения больных с гнойно-некротическими осложнениями деструктивного панкреатита.
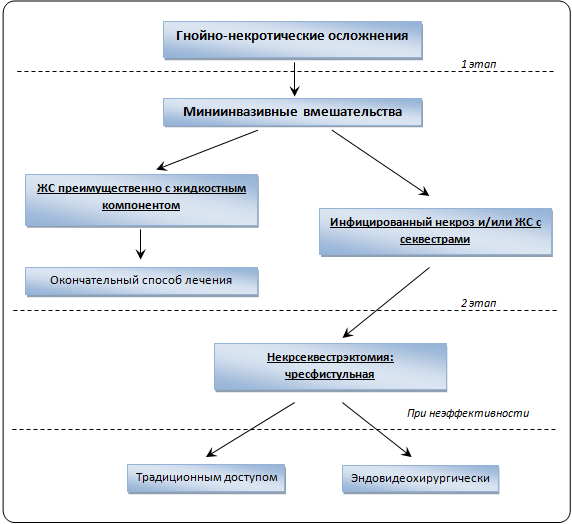
Таким образом, у больных с гнойно-некротическими осложнениями деструктивного панкреатита первым этапом всегда возможно выполнение миниинвазивных вмешательств под контролем УЗИ и РТВ. Однако, при сохраняющемся интоксикационном синдроме, в течение 20 суток послеоперационного периода необходимо решение вопроса об адекватной некрсеквестрэктомии открытым или эндовидеохирургическим доступом с целью сохранения минимально травматичного подхода в лечении. При этом оперативное вмешательство будет проходить в более благоприятных условиях, поскольку к этому времени произойдет отграничение зоны некроза от здоровых тканей.
ВЫВОДЫ
1.
Развитие клинико-лабораторных проявлений
интоксикационного синдрома во второй фазе течения деструктивного панкреатита
соответствует появлению ряда новых УЗ-признаков, характерных для
гнойно-некротических осложнений.
2.
Методически последовательное УЗИ позволяет
выявить особенности и оценить распространенность деструктивного процесса,
проследить динамику развития гнойно-некротических осложнений и уточнить
рациональный объем оперативного вмешательства.
3.
Миниинвазивные вмешательства под рентгенотелевизионным
и ультразвуковым контролем являются эффективным способом удаления жидкостных
скоплений, профилактики прогрессирования гнойно-некротического процесса в клетчаточных
пространствах. Они могут выполняться как в качестве первого этапа, так и быть
окончательным методом хирургического лечения.
4.
У 79,2% больных чрескожные миниинвазивные
вмешательства оказались окончательным способом дренирования и
некрсеквестрэктомии. Наилучшие результаты отмечены у больных, имевших единичные
жидкостные скопления с флюктуирующим (гнойным) содержимым. Менее эффективными
вмешательства были у пациентов с инфицированным некрозом без жидкостного
компонента и жидкостными скоплениями с преимущественно некротическим
компонентом (секвестрами).
5.
В сравнимых группах мининвазивные
вмешательства по сравнению с традиционными операциями имеют более благоприятное
течение послеоперационного периода за счет сохранения отграничения очага
воспаления и менее выраженного возврата интоксикации. Это приводит к уменьшению
числа осложнений и летальности. Однако значительное увеличение койко-дня до
70,9±6,7 ведет к ограничению использования методики в
условиях современных медикоэкономических стандартов и делает целесообразным
использование различных комбинаций чрескожных и открытых вмешательств.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1.
При первичном осмотре УЗИ следует
выполнять в полном объеме, осуществляя сканирование всех органов и систем
брюшной полости, клетчаточных пространств, плевральных синусов. Последующий
мониторинг должен осуществляться не реже одного раза в 1-3 сут. В процессе
лечения УЗИ является оптимальным методом для оценки результатов и необходимости
хирургического вмешательства.
2.
При дренировании жидкостных скоплений с
преимущественно жидкостным компонентом возможно использование методики
«стилет-катетер» и дренажей небольшого диаметра размером до 14 Fr.
3.
При выполнении миниинвазивных вмешательств
по поводу жидкостных скоплений с преимущественно некротическим компонентом
(секвестрами) внебрюшинный доступ является предпочтительным, однако, при
отсутствии такового возможен доступ через брюшную полость. Дренирование
необходимо осуществлять по методике Сельдингера дренажами большого диаметра
типа «корзина» с целью последующего удаления секвестров.
4.
Для улучшения результатов чрескожного
пункционно-дренажного лечения необходима ежедневная санация полостей
деструкции, постоянный контроль положения дренажей и адекватности дренирования.
5.
Этапные чресфистульные секвестрэктомии
целесообразно выполнять в условиях рентгеноперационной для контроля полноты
удаления секвестров.
6.
Проточное промывание инфицированных зон
деструкции производить не рекомендуется вследствие риска обтурации дренажа
крупным секвестром и возможностью распространения инфекции по забрюшинной
клетчатке.
7.
В случаях сохранения синдрома интоксикации
необходимо использование лучевых методов исследования (УЗИ и фистулографии) с
целью выявления недренируемых затеков.
8.
При сохранении интоксикационного синдрома
в течение длительного времени после дренирования необходимо решение вопроса о традиционном
оперативном вмешательстве с целью проведения полноценной некрсеквестрэктомии.
Список работ, опубликованных по теме диссертации
1. Кубышкин
В.А., Кулезнева Ю.В., Мороз О.В. Роль
чрескожных вмешательств под ультразвуковым и рентгенологическим контролем в
лечении деструктивного панкреатита. Материалы науч.-практ. конф. «Чрескожные и
внутрипросветные эндоскопические вмешательства в хирургии» 2010; 95-96.
2. Мороз О.В.,
Кулезнева Ю.В., Израилов Р.Е. Чрескожное цистогастральное дренирование
постнекротических кист поджелудочной железы. Сборник научных трудов V межрегиональной конференции,
посвященной памяти академика РАМН профессора Л.В. Полуэктова «Актуальные
проблемы хирургии» 2011; 16-18.
3. Мороз О.В.,
Кулезнева Ю.В., Израилов Р.Е. Диагностика и лечение постнекротических кист
поджелудочной железы под ультразвуковым и эндоскопическим контролем. Российский журнал гастроэнтерологии,
гепатологии, колопроктологии. 2011; XXI: 163.
4. Кулезнева
Ю.В., Мороз О.В., Израилов Р.Е. Чрескожные
вмешательства при гнойно-некротических осложнениях деструктивного панкреатита.
Материалы VI Всероссийского национального конгресса лучевых диагностов и
терапевтов. Радиология – 2012;
5. Кубышкин
В.А., Мороз О.В., Степанова Ю.А., Кармазановский Г.Г., Кулезнева
Ю.В. Вопросы классификации острого панкреатита. Анналы хирургической гепатологии. 2012; 17(.2): 86-94.
6. Мороз О.В.,
Кулезнева Ю.В., Степанова Ю.А. Миниинвазивное лечение гнойно-некротических
осложнений панкреонекроза. Сборник трудов IX научно практической конференции
радиологов Узбекистана «Современные методы медицинской визуализации и
интервенционной радиологии». 20012; 110.
7. Мороз О.В.,
Кулезнева Ю.В., Степанова Ю.А. Миниинвазивное лечение гнойно-некротических
осложнений острого деструктивного панкреатита. Вестник хирургической гастроэнтерологии. 2012; Приложение: 53.
8.
Kuleznyova Yu., Moroz O., Dubrovsky A., Stepanova Yu. Purulent-necrotic
complications of acute destructive pancreatitis: possibilities of radiology
diagnostics in definition of treatment tactics. Book of abstracts of 10th Congress of
European-African Hepato Pancreato Biliary Association,
9. Кулезнева Ю.В., Охотников
О.И., Мусаев Г.Х., Израилов Р.Е., Бруслик С.В., Григорьев С.Н., Мороз О.В. Чрескожное внутреннее дренирование постнекротических
кист поджелудочной железы. Анналы
хирургической гепатологии. 2012; 17(4): 49-56.
10.
Кулезнева Ю.В., Мороз О.В., Степанова Ю.А.
Миниинвазивное лечение гнойно-некротических осложнений деструктивного
панкреатита». Сборник материалов XX международного Конгресса Ассоциации
хирургов-гепатологов стран СНГ «Актуальные проблемы хирургической гепатологии»,
Донецк, 18 – 20 сентября 2013 года; 192.
11.
Кубышкин
В.А., Мороз О.В., Степанова Ю.А.,
Кармазановский Г.Г., Кулезнева Ю.В. Гнойно-некротические осложнения острого
деструктивного панкреатита: возможности лучевых методов диагностики в
определении тактики лечения (часть 1). Диагностическая
и интервенционная радиология. 2013; 3: 81-94.